Licenca
To delo je na voljo pod pogoji slovenske licence Creative Commons 2.5:
priznanje avtorstva - nekomercialno - deljenje pod enakimi pogoji.
Celotna licenca je na voljo na spletu na naslovu http://creativecommons.org/licenses/by-nc-sa/2.5/si/. V skladu s to licenco je dovoljeno vsakemu uporabniku delo razmnoževati, distribuirati, javno priobčevati, dajati v najem in tudi predelovati, vendar samo v nekomercialne namene in ob pogoju, da navede avtorja oziroma avtorje in izdajatelja tega dela. Če uporabnik delo predela, kar pomeni, da ga spremeni, preoblikuje, prevede ali uporabi to delo v svojem delu, lahko predelavo dela ponudi na voljo le pod pogoji, ki so enaki pogojem iz te licence oziroma pod enako licenco.

priznanje avtorstva - nekomercialno - deljenje pod enakimi pogoji.
Celotna licenca je na voljo na spletu na naslovu http://creativecommons.org/licenses/by-nc-sa/2.5/si/. V skladu s to licenco je dovoljeno vsakemu uporabniku delo razmnoževati, distribuirati, javno priobčevati, dajati v najem in tudi predelovati, vendar samo v nekomercialne namene in ob pogoju, da navede avtorja oziroma avtorje in izdajatelja tega dela. Če uporabnik delo predela, kar pomeni, da ga spremeni, preoblikuje, prevede ali uporabi to delo v svojem delu, lahko predelavo dela ponudi na voljo le pod pogoji, ki so enaki pogojem iz te licence oziroma pod enako licenco.

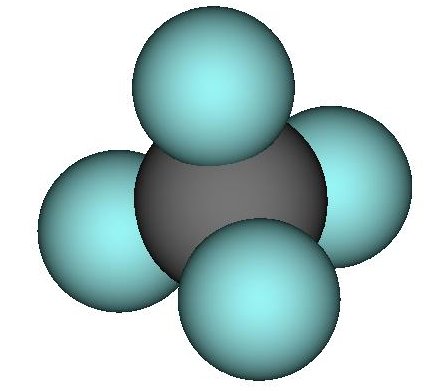 Prikazan je kalotni model ogljikovega tetrafluorida (CF4). Kolikšen je masni delež fluora v tej spojini? Dopolnite besedilo. Relativno atomsko in relativno molekulsko maso zapišite kot celo število, masni delež pa zapišite na dve decimalni mesti natančno (dve števki za decimalno vejico).
Prikazan je kalotni model ogljikovega tetrafluorida (CF4). Kolikšen je masni delež fluora v tej spojini? Dopolnite besedilo. Relativno atomsko in relativno molekulsko maso zapišite kot celo število, masni delež pa zapišite na dve decimalni mesti natančno (dve števki za decimalno vejico).